氨基酸分析过程中前处理方法的选择及优化
在所检测氨基酸样品中,有的样品中氨基酸以游离态存在,而有的样品中氨基酸以蛋白或多肽形式存在,当然,大多数样品氨基酸以两种形式同时存在。根据关注点不同,我们常常把样品分为游离样品和水解样品。
水解样品前处理技术
水解技术适用于氨基酸以蛋白或多肽形式存在的样品,氨基酸主要是以肽键结合,需要设法将肽键打开,水解成单个游离氨基酸,而当前还没有哪一种水解剂能将所有的氨基酸毫无破坏的水解出来,这就决定了氨基酸总量测定前处理方法的复杂性和多样性。
常用的水解方法分为:盐酸水解法、磺酸水解法、酶水解法、过甲酸氧化法和碱水解法。由于酸水解对色氨酸完全破坏,而胱氨酸水解成半胱氨酸,后者不能与茚三酮产生颜色反应;所以碱水解法是测定色氨酸最有效的方法,过甲酸氧化法只是用来测定胱氨酸。
游离氨基酸测定样品的制备
游离氨基酸测定样品从形态上可分为两大类:液体样品和固体样品。测定游离氨基酸的样品,主要需要考去除杂质。如果氨基酸存在于组织等固体样品中,则需要从样品中中把氨基酸提取出来并去除杂质。杂质主要包括蛋白质和金属离子,金属离子用EDTA去除,蛋白沉淀剂应用较多的有三氯乙酸法、苦味酸、磺基水杨酸(SAA)法、乙醇沉淀法、超速离心法等,经过对蛋白沉淀实验比较,发现采用三氯乙酸法相比较其他方法去蛋白效果更好。脂肪含量高的样品仍需先用乙醚或者石油醚脱脂。
影响水解因素及其优化
1.样品的性质
纯蛋白样品水解影响因素较小,而对含碳水化合物较多的如饲料样品就会因碳水化合物而回收率降低,使水解方法受到限制。如在盐酸水解时纯蛋白质中的蛋氨酸损失很小,而谷类样品中的蛋氨酸则会损失20-30%,如果此时在酸中加入巯基试剂,谷类样品中的蛋氨酸回收率就会大大提高,一般是碳水化合物越多,回收率也就越高。
2.水解试剂的选择
因对蛋白质中20种氨基酸有极强的水解能力,所以最常用的水解剂是盐酸;对特殊要求如测定色氨酸时,最好选择碱做水解剂。如果在酸水解液中加入保护剂巯基乙醇可以提高胱氨酸和蛋氨酸的回收率;如要提高酪氨酸的回收率则应在盐酸中加入酚类化合物。如果要测定酰胺类化合物,应选用蛋白酶作水解液。怎么样选择水解液,最好要根据氨基酸的特性来选择。
3.水解液的使用量
一般采用相当于蛋白质重量500-5000倍的6mol盐酸,相对加大6mol盐酸与蛋白质重量的比例,可以避免氨基酸水解的损失,也就是说,水解液越多,对氨基酸的破坏越小。
4.水解的真空度
水解管中含氧量在有空气存在的情况下,含硫氨基酸由于氧化而有较大损失,如酸水解可使蛋氨酸损失可达20-30%,酪氨酸和组氨酸也会损失10%左右。因此在水解管封管前要先充满高纯氮气,再封管。
5.水解时间的影响
不同氨基酸形成的肽键对水解液反应不同,完全水解所需时间也会不同,缬、异亮肽键不易水解,72小时才能达到最大值,而胱氨酸、苏氨酸、丝氨酸、酪氨酸、苯丙氨酸、蛋氨酸等氨基酸随水解时间延长而逐渐破坏,水解时间越长,回收率也就越低。24小时是取一个相当于固定大的多数氨基酸回收率都较高的一个时间。
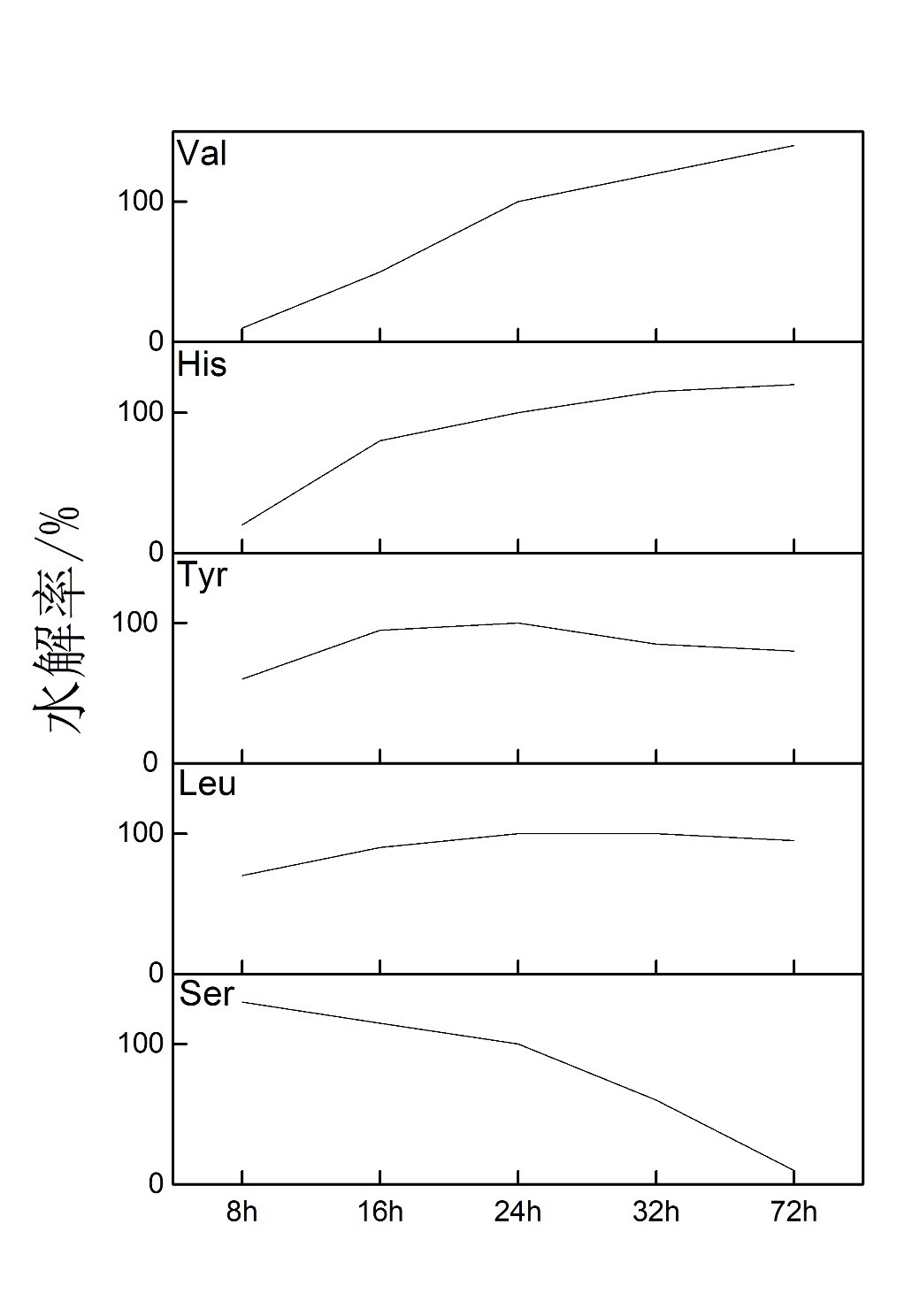
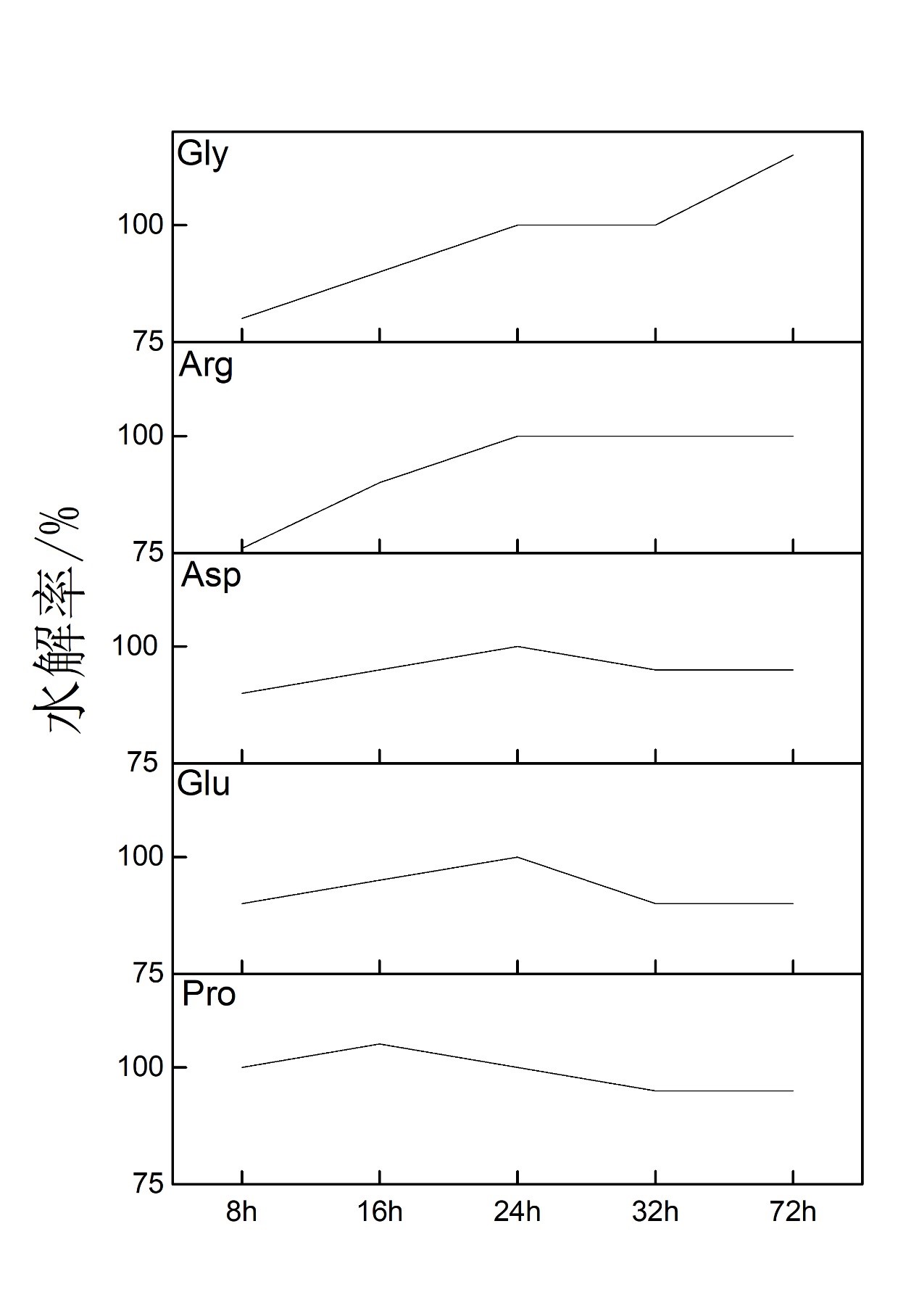
6.水解温度的选择
水解温度过低会使水解不完全,温度太高又会使有极性侧链的氨基酸如苏氨酸、丝氨酸等破坏。常用水解温度是110℃,水解时间为22-24小时。也可以适当提高水解的温度,能缩减水解时间,提高工作效率,如用140℃高温水解,仅水解4-5小时实验结果就与110℃条件下24小时水解结果相似。
在酸水解当中。一些氨基酸的破坏可以用实验值来进行校正。一种是用与水解蛋白质样品相同条件情况下来水解已知含量的氨基酸混合标准,用测定值来校正蛋白质水解后的氨基酸数值。例如110℃条件下6mol盐酸水解24小时的Arg精氨酸回收率为95.5%,Leu亮氨酸回收率为96.2%,Ser丝氨酸回收率为92.7%等。另一种方法是用已知含量和组成的纯蛋白质,在相同条件下进行水解,用测定值得到各个氨基酸的回收率,用来去校正分析数据。
撰稿人 俞立东
附件下载:
 鲁公网安备37020202001323号
鲁公网安备37020202001323号 